class 10 - Science Notes
Chapter 1 -रासायनिक अभिक्रियाएँ एवं समीकरण
यह अध्याय कक्षा 10 विज्ञान के सबसे महत्वपूर्ण अध्यायों में से एक है। इस अध्याय से बोर्ड परीक्षा में हर वर्ष 6–10 अंक तक के प्रश्न पूछे जाते हैं।
इस अध्याय में रासायनिक अभिक्रिया, उनके प्रकार, रासायनिक समीकरण,
संक्षारण और विकर्षण जैसे महत्वपूर्ण विषयों को सरल भाषा में समझाया गया है।
इस अध्याय में आप निम्नलिखित विषय सीखेंगे:
• रासायनिक अभिक्रिया की परिभाषा
• रासायनिक समीकरण और उनके प्रकार
• अभिक्रियाओं के उदाहरण
• संक्षारण (Corrosion)
• विकर्षण (Rancidity)
नीचे दिए गए प्रश्न कक्षा 10 बोर्ड परीक्षा के लिए अत्यंत महत्वपूर्ण हैं और NCERT के अनुसार तैयार किए गए हैं।
1. रासायनिक अभिक्रिया क्या है?
परिभाषा:
जब दो या दो से अधिक पदार्थ मिलकर एक नया पदार्थ बनाते हैं
जिसके गुण मूल पदार्थों से भिन्न होते हैं, तो उसे रासायनिक अभिक्रिया कहते हैं।
सरल शब्दों में:
जब किसी पदार्थ की पहचान बदल जाए, तो समझिए रासायनिक अभिक्रिया हुई है।
पहचान: अवस्था में परिवर्तन, रंग में परिवर्तन, गैस का निकलना, या तापमान में परिवर्तन।
उदाहरण: दूध से दही बनना, लोहे पर जंग लगना, भोजन का पचना।
2. रासायनिक समीकरण (Chemical Equation)
अभिक्रिया को प्रतीकों (Symbols) और सूत्रों (Formulas) के माध्यम से लिखना।
संतुलित समीकरण क्यों जरूरी है?
क्योंकि रासायनिक अभिक्रिया में द्रव्यमान संरक्षण का नियम लागू होता है।
बोर्ड परीक्षा में असंतुलित और संतुलित समीकरण में अंतर पूछा जा सकता है।
असंतुलित (Skeletal) समीकरण: $$Mg + O_2 \rightarrow MgO$$ (यह गलत है क्योंकि द्रव्यमान बराबर नहीं है)।
संतुलित (Balanced) समीकरण: $$2Mg + O_2 \rightarrow 2MgO$$
संतुलित करना क्यों जरूरी है? ‘द्रव्यमान संरक्षण के नियम’ (Law of Conservation of Mass) के अनुसार, द्रव्यमान न तो बनाया जा सकता है और न ही नष्ट किया जा सकता है। इसलिए दोनों तरफ परमाणुओं की संख्या बराबर होनी चाहिए।
3. रासायनिक अभिक्रियाओं के प्रकार (Types of Chemical Reactions)
📌 बोर्ड परीक्षा नोट:
रासायनिक अभिक्रिया की पहचान से 1 अंक का प्रश्न लगभग हर साल पूछा जाता है।
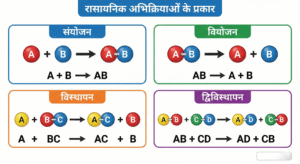
यह इस चैप्टर का सबसे महत्वपूर्ण हिस्सा है:
(क) संयोजन अभिक्रिया (Combination Reaction)
जब दो या दो से अधिक अभिकारक मिलकर एकल उत्पाद (Single Product) बनाते हैं।
सूत्र: $$A + B \rightarrow C$$
उदाहरण: कोयले का दहन ($$C + O_2 \rightarrow CO_2$$)
महत्वपूर्ण: बिना बुझा चूना ($$CaO$$) जब पानी के साथ मिलता है तो बुझा हुआ चूना ($$Ca(OH)_2$$) बनाता है और बहुत सारी ऊष्मा (Heat) निकलती है। इसे ऊष्माक्षेपी (Exothermic) अभिक्रिया भी कहते हैं।
(ख) वियोजन/अपघटन अभिक्रिया (Decomposition Reaction)
जब एक एकल अभिकारक टूटकर दो या अधिक उत्पाद बनाता है। इसके लिए ऊर्जा की जरूरत होती है (ऊष्माशोषी/Endothermic)। यह तीन तरह से होता है:
ऊष्मीय (Thermal): गर्मी देने पर। (जैसे $CaCO_3$ को गर्म करने पर $CaO + CO_2$ बनता है)।
वैद्युत (Electrolytic): बिजली गुजारने पर। ($2H_2O \rightarrow 2H_2 + O_2$)।
प्रकाशीय (Photolytic): सूर्य के प्रकाश में। ($2AgCl \rightarrow 2Ag + Cl_2$)। इसका उपयोग श्याम-श्वेत फोटोग्राफी (Black & White Photography) में होता है।
(ग) विस्थापन अभिक्रिया (Displacement Reaction)
जब अधिक क्रियाशील तत्व (More Reactive Element), कम क्रियाशील तत्व को उसके यौगिक से हटा देता है।
उदाहरण: लोहे की कील को कॉपर सल्फेट के नीले विलियन में डालने पर वह हरा हो जाता है।
समीकरण: $Fe(s) + CuSO_4(aq) \rightarrow FeSO_4(aq) + Cu(s)$
(लोहा, कॉपर से ज्यादा ताकतवर है, इसलिए उसने कॉपर को हटा दिया)।
(घ) द्विविस्थापन अभिक्रिया (Double Displacement Reaction)
इसमें अभिकारकों के बीच आयनों (Ions) का आदान-प्रदान होता है।
अवक्षेपण (Precipitation): अक्सर इसमें एक ऐसा पदार्थ बनता है जो पानी में नहीं घुलता (इसे अवक्षेप कहते हैं)।
उदाहरण: $Na_2SO_4 + BaCl_2 \rightarrow BaSO_4 (\text{Safed Avakshep}) + 2NaCl$
(ङ) उपचयन और अपचयन (Oxidation and Reduction)
उपचयन (Oxidation): ऑक्सीजन का जुड़ना या हाइड्रोजन का हटना।
अपचयन (Reduction): ऑक्सीजन का हटना या हाइड्रोजन का जुड़ना।
रेडॉक्स (Redox): जब एक ही अभिक्रिया में एक का उपचयन और दूसरे का अपचयन हो रहा हो।
$CuO + H_2 \xrightarrow{\text{Heat}} Cu + H_2O$
(यहाँ $CuO$ से ऑक्सीजन हटी तो अपचयन, और $H_2$ में ऑक्सीजन जुड़ी तो उपचयन)।
4. दैनिक जीवन में उपचयन के प्रभाव
संक्षारण (Corrosion): जब धातु नमी या एसिड के संपर्क में आकर कमजोर हो जाती है। (जैसे- लोहे पर जंग लगना, चांदी का काला पड़ना, तांबे पर हरी परत चढ़ना)।
बचाव: पेंट करना, तेल लगाना, यशदलेपन (Galvanisation)।
विकृतगंधिता (Rancidity): वसा युक्त खाना (जैसे चिप्स) हवा के संपर्क में आने पर खराब हो जाता है और बदबू आने लगती है।
बचाव: चिप्स के पैकेट में नाइट्रोजन गैस भरी जाती है (क्योंकि यह कम सक्रिय है) या वायुरोधी बर्तन इस्तेमाल किए जाते हैं।
🔹 इस अध्याय का सारांश:
• रासायनिक अभिक्रिया में नए पदार्थ बनते हैं
• समीकरण संतुलित होना आवश्यक है
• संक्षारण धातुओं को नुकसान पहुँचाता है
• विकर्षण भोजन को खराब करता है
निष्कर्ष:
रासायनिक अभिक्रियाएँ हमारे दैनिक जीवन का अभिन्न भाग हैं।
इस अध्याय की अच्छी समझ से विद्यार्थी न केवल बोर्ड परीक्षा
बल्कि आगे की कक्षाओं के लिए भी मजबूत आधार बना सकते हैं।
🔗 संबंधित अध्याय: Notes
- Chapter 2 – अम्ल, क्षार और लवण
- Chapter 3 – धातु और अधातु
- Chapter 4 – कार्बन एवं उसके यौगिक
- Chapter 5 – जैव प्रक्रम
- Chapter 6 – नियंत्रण एवं समन्वय
- Chapter 7 – जीव जनन कैसे करते हैं
- Chapter 8 – आनुवंशिकता एवं जैव विकास
- Chapter 9 – प्रकाश – परावर्तन तथा अपवर्त
- Chapter 10 – मानव नेत्र तथा रंगीन संसार
- Chapter 11 – विद्युत
- Chapter 12 – विद्युत धारा के चुंबकीय प्रभाव
- Chapter 13 – हमारे पर्यावरण